Ghi nhớ công thức tính nội năng và các dạng biến thiên cơ bản
Công thức tính nội năng giúp xác định năng lượng bên trong của vật chất. Các phương trình toán học đơn giản mô tả mối liên hệ giữa nhiệt độ và trạng thái vật chất. Giáo viên hướng dẫn chi tiết cách áp dụng công thức cho từng dạng chất khí, lỏng và rắn.
Công thức tính nội năng và ý nghĩa vật lý
Nội năng là tổng động năng và thế năng của các phân tử trong vật. Công thức tính nội năng được xác định dựa trên nhiệt độ và số bậc tự do của phân tử.
Đối với khí lý tưởng đơn nguyên tử, công thức tính nội năng là:
U = (3/2)nRT
Trong đó:
- U: nội năng (J)
- n: số mol chất khí (mol)
- R: hằng số khí (8,31 J/mol.K)
- T: nhiệt độ tuyệt đối (K)
Với khí lý tưởng đa nguyên tử, công thức có dạng:
U = (i/2)nRT
Trong đó i là số bậc tự do của phân tử:
- i = 3 với khí đơn nguyên tử
- i = 5 với khí hai nguyên tử
- i = 6 với khí đa nguyên tử
Ý nghĩa vật lý của nội năng thể hiện qua việc đo lường năng lượng bên trong của hệ. Khi nhiệt độ tăng, các phân tử chuyển động nhanh hơn làm tăng động năng và nội năng.
Kinh nghiệm giảng dạy cho thấy học sinh thường nhầm lẫn giữa i và n trong công thức. Cách dễ nhớ là i luôn là số chẵn từ 3-6 còn n là số mol có thể là số thập phân.
Ví dụ: Tính nội năng của 2 mol khí O2 ở 27°C.
- O2 là khí 2 nguyên tử nên i = 5
- T = 27 + 273 = 300K
- U = (5/2) × 2 × 8,31 × 300 = 12.465J
Nội năng và các yếu tố ảnh hưởng đến nội năng của vật chất
Nội năng phụ thuộc vào đâu là câu hỏi thường gặp khi học về nhiệt động lực học. Nội năng là tổng động năng và thế năng của các phân tử cấu tạo nên vật chất.
Để hiểu rõ hơn về nội năng, ta cần tìm hiểu các khái niệm cơ bản và các yếu tố tác động đến đại lượng này.
Khái niệm nội năng trong nhiệt động lực học
Nội năng trong nhiệt động lực học là năng lượng của hệ nhiệt động, bao gồm động năng chuyển động hỗn loạn của các phân tử và thế năng tương tác giữa chúng.
Công thức tính nội năng:
U = Ek + Ep
Trong đó:
- U: nội năng của hệ (J)
- Ek: động năng của các phân tử (J)
- Ep: thế năng tương tác giữa các phân tử (J)
Khi giảng dạy, tôi thường ví von nội năng như “két tiền” của hệ nhiệt động
- nơi tích trữ năng lượng bên trong vật chất.
Các yếu tố ảnh hưởng đến nội năng
Nội năng của một hệ phụ thuộc vào nhiều yếu tố khác nhau. Khối lượng và bản chất của chất là hai yếu tố quan trọng nhất.
Với cùng một loại chất, khối lượng càng lớn thì nội năng càng cao. Điều này tương tự như công thức độ tự cảm phụ thuộc vào số vòng dây của cuộn dây.
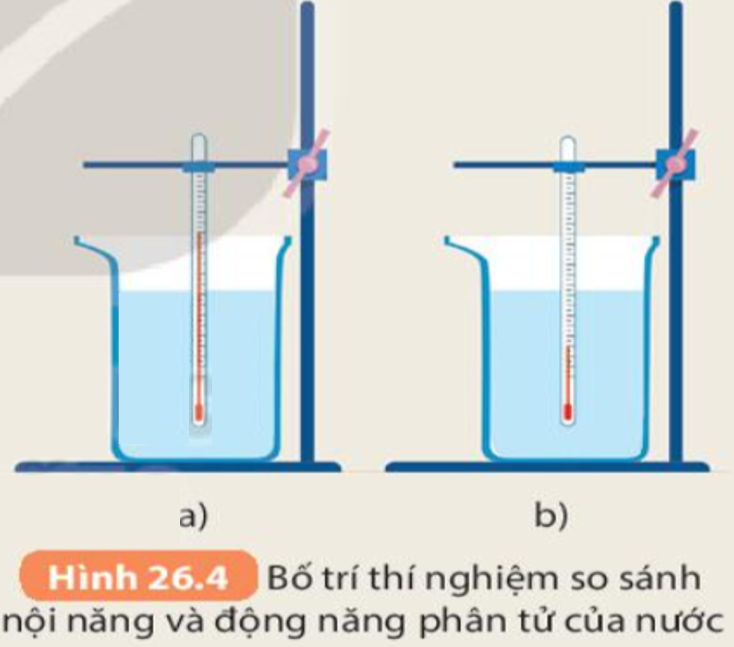
Bản chất của chất quyết định cấu trúc phân tử và lực tương tác giữa các phân tử, từ đó ảnh hưởng trực tiếp đến thế năng của hệ.
Mối quan hệ giữa nội năng và nhiệt độ
Nhiệt độ và nội năng có mối quan hệ tỷ lệ thuận với nhau. Khi nhiệt độ tăng, động năng chuyển động của các phân tử tăng.
Công thức biểu diễn mối quan hệ:
ΔU = mcΔT
Trong đó:
- ΔU: độ biến thiên nội năng (J)
- m: khối lượng chất (kg)
- c: nhiệt dung riêng (J/kg.K)
- ΔT: độ biến thiên nhiệt độ (K)
Qua 20 năm giảng dạy, tôi nhận thấy học sinh thường nhầm lẫn giữa nhiệt độ và nội năng. Nhiệt độ chỉ phản ánh mức độ chuyển động của phân tử, còn nội năng là tổng năng lượng của toàn hệ.
Công thức tính nội năng cho các trạng thái vật chất
Nội năng là tổng động năng và thế năng của các phân tử trong vật chất. Mỗi trạng thái vật chất có công thức tính nội năng khác nhau.
Tôi sẽ giải thích chi tiết cách tính công thức tính nội năng cho từng trạng thái vật chất. Việc nắm vững các công thức này giúp giải quyết nhiều bài tập về nhiệt động lực học.
Nội năng của chất khí
Nội năng của chất khí được tính dựa trên số bậc tự do của phân tử. Công thức tổng quát:

U = (i/2)nRT
Trong đó:
- i: số bậc tự do của phân tử khí
- n: số mol chất khí
- R: hằng số khí (8,31 J/mol.K)
- T: nhiệt độ tuyệt đối (K)
Với khí đơn nguyên tử i=3, khí lưỡng nguyên tử i=5, khí đa nguyên tử i=6.
Nội năng của chất lỏng
Nội năng của chất lỏng phức tạp hơn do có lực tương tác giữa các phân tử. Công thức:
U = mcΔT + mL
Trong đó:
- m: khối lượng chất lỏng
- c: nhiệt dung riêng
- ΔT: độ chênh lệch nhiệt độ
- L: nhiệt ẩn hóa hơi
Chất lỏng có thể chuyển pha nên cần tính thêm nhiệt ẩn hóa hơi L.
Nội năng của chất rắn
Nội năng của chất rắn được tính dựa trên dao động của các nguyên tử mạng tinh thể:
U = 3NkT
Trong đó:
- N: số nguyên tử trong tinh thể
- k: hằng số Boltzmann
- T: nhiệt độ tuyệt đối
Đây là mô hình Einstein về nhiệt dung của chất rắn. Thực tế, ở nhiệt độ thấp cần dùng mô hình Debye phức tạp hơn.
Biến thiên nội năng và phương pháp tính
Biến thiên nội năng là một khái niệm quan trọng trong nhiệt động lực học. Nó cho biết sự thay đổi năng lượng bên trong của một hệ nhiệt động. Việc nắm vững cách tính biến thiên nội năng giúp giải quyết nhiều bài toán về nhiệt.
Khái niệm biến thiên nội năng
Biến thiên nội năng là độ chênh lệch giữa nội năng cuối và nội năng đầu của một hệ. Nó phản ánh sự thay đổi năng lượng bên trong của hệ khi trải qua một quá trình nhiệt động.
Trong quá trình giảng dạy, tôi thường ví von biến thiên nội năng như việc kiểm tra số tiền trong ví trước và sau khi mua sắm. Sự chênh lệch này cho biết bạn đã chi tiêu bao nhiêu.
Công thức tính biến thiên nội năng
Công thức độ biến thiên nội năng được biểu diễn:
ΔU = U2
Trong đó:
- ΔU: Biến thiên nội năng (J)
- U2: Nội năng cuối (J)
- U1: Nội năng đầu (J)
Một cách tính khác dựa vào nguyên lý I nhiệt động học:
ΔU = Q
Với Q là nhiệt lượng hệ nhận vào và A là công hệ sinh ra.
Ví dụ minh họa và bài tập áp dụng
Xét một khối khí lý tưởng được đun nóng ở thể tích không đổi:
- Nhiệt lượng nhận vào Q = 100J
- Công sinh ra A = 0J (do thể tích không đổi)
- Áp dụng công thức: ΔU = 100
- 0 = 100J
Như vậy, nội năng của khối khí tăng thêm 100J. Đây là một ví dụ điển hình tôi thường dùng để giúp học sinh hiểu rõ về biến thiên nội năng.
Khi giải các bài tập, cần xác định rõ:
- Trạng thái đầu và cuối của hệ
- Nhiệt lượng trao đổi
- Công sinh ra trong quá trình
FAQ: Câu hỏi thường gặp về nội năng
Nội năng là một khái niệm quan trọng trong nhiệt động lực học. Tôi sẽ giải đáp những thắc mắc phổ biến về nội năng mà học sinh thường gặp phải.
Công thức nội năng là gì và cách áp dụng?
Công thức nội năng được biểu diễn bằng U = Q + A, trong đó:
- U là nội năng của hệ
- Q là nhiệt lượng hệ nhận được
- A là công ngoài tác dụng lên hệ
Khi áp dụng công thức, cần xác định rõ chiều của nhiệt lượng và công. Nếu hệ nhận nhiệt thì Q > 0, ngược lại Q < 0. Tương tự, nếu môi trường sinh công lên hệ thì A > 0.
Trong thực tế giảng dạy, tôi thường hướng dẫn học sinh phân tích kỹ bài toán để xác định đúng dấu của Q và A trước khi tính toán.
Làm thế nào để tính nội năng chính xác?
Để tính cách tính nội năng vật chất chính xác, ta cần:
Xác định rõ trạng thái đầu và cuối của hệ. Điều này giúp tính được sự biến thiên nội năng ΔU.
Phân tích các quá trình xảy ra với hệ:
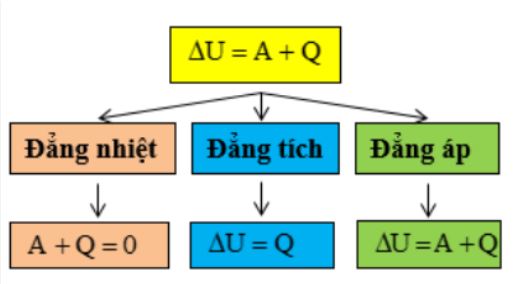
- Quá trình đẳng tích: ΔU = Q
- Quá trình đẳng nhiệt: ΔU = 0
- Quá trình đoạn nhiệt: Q = 0
Kinh nghiệm của tôi là vẽ đồ thị p-V để hình dung rõ quá trình biến đổi của hệ.
Những sai lầm thường gặp khi tính nội năng
Công thức tính nội năng thường bị nhầm lẫn khi:
Không phân biệt được chiều của nhiệt lượng và công. Nhiều học sinh cộng cả Q và A dương vào công thức mà không xét dấu.
Áp dụng sai công thức cho từng quá trình. Ví dụ với quá trình đẳng nhiệt, vẫn tính ΔU khác 0.
Qua 20 năm giảng dạy, tôi nhận thấy việc hiểu rõ bản chất vật lý quan trọng hơn việc nhớ máy móc công thức.
Việc áp dụng đúng công thức tính nội năng giúp xác định chính xác năng lượng bên trong của vật chất. Các công thức tính nội năng cho chất khí, lỏng, rắn đều tuân theo nguyên lý bảo toàn năng lượng và phụ thuộc vào nhiệt độ. Biến thiên nội năng phản ánh sự thay đổi trạng thái của hệ nhiệt động. Giáo viên cần hướng dẫn học sinh nắm vững công thức cơ bản và phương pháp tính toán để giải quyết các bài toán về nội năng một cách hiệu quả.
Bài viết liên quan

Học công thức khí lý tưởng và các định luật cơ bản trong hóa học
Tìm hiểu công thức khí lý tưởng và các định luật liên quan qua phương pháp giảng dạy đơn giản. Bao gồm điều kiện, đặc điểm, bài tập mẫu và hướng dẫn giải chi tiết.

Học thuộc công thức tính nhiệt nóng chảy và ứng dụng trong hóa học
Tìm hiểu công thức tính nhiệt nóng chảy và các khái niệm cơ bản về nhiệt nóng chảy riêng, đơn vị đo, bảng tra cứu các chất thông dụng. Hướng dẫn chi tiết cách tính và ứng dụng thực tế.

Công thức đoạn nhiệt khái quát và cách áp dụng trong hóa học cơ bản
Tìm hiểu chi tiết về công thức đoạn nhiệt trong hóa học với cách tính, phương pháp xác định và ứng dụng. Bài viết giải thích đơn giản các khái niệm đoạn nhiệt chuẩn, phản ứng kèm bài tập mẫu.

Điểm qua công thức tính công suất tỏa nhiệt và ứng dụng thực tế
Tìm hiểu chi tiết công thức tính công suất tỏa nhiệt trong mạch điện với các khái niệm cơ bản, công thức Q=I²Rt và ứng dụng thực tế qua bài tập có lời giải mẫu đơn giản.

Nắm kỹ công thức tính nhiệt độ tuyệt đối và cách chuyển đổi thang nhiệt
Tìm hiểu công thức tính nhiệt độ tuyệt đối và cách chuyển đổi giữa độ C, K. Giải thích chi tiết khái niệm, ứng dụng thực tế cùng bài tập minh họa về thang nhiệt Kelvin.

Học công thức đẳng nhiệt và ứng dụng trong khí lý tưởng cơ bản
Tìm hiểu chi tiết công thức đẳng nhiệt và định luật Boyle-Mariotte qua các ví dụ, bài tập có lời giải. Phân tích đồ thị, ứng dụng thực tế giúp nắm vững kiến thức cơ bản.

